海外疫情爆发
受奥密克戎全球大流行影响,全球确诊病例数近期呈现攀升态势。国家卫健委新闻发言人米锋15日在国务院联防联控机制新闻发布会上曾表示,1月以来,全球新冠肺炎日新增确诊病例最高已突破350万例。据世卫组织简报,过去30天,全球上传的基因序列中,58.5%为奥密克戎毒株,该毒株传播快、传染力强,正在迅速取代其它变异株。
数据显示,美国、法国、印度、意大利、澳大利亚是新增确诊病例数最多的五个国家。
新冠病毒自测盒需求大增
一系列变动之下,新冠自测盒在重走2020年疫情之初口罩、手套等防疫物资大火的旧路。新冠病毒自测盒已经在美遭遇抢购和抬价。美国联邦贸易委员会(FTC)在近期还警告美国人,不要使用假的家用检测试剂盒。

早在去年12月,拜登政府就宣布将自2022年1月份开始,向美国民众免费发放5亿份家用快速检测试剂盒。1月10日,美国白宫宣布该计划将于1月15日实施,开始由保险公司承保,每月为每位受保人报销最多8次非处方居家新冠检测的费用,每次不超过12美,也就是说在拥有3.3亿人口的美国,粗略估算,政府每月免费向民众发放试剂盒的量约为26亿份。
什么是新冠快速自测试剂盒?
新冠快速自测试剂盒与国内的新冠核酸检测原理不同,一般采用抗原、抗体检测试剂,具有检测速度快、不需要专业设备和人员、准确度将对较高、适合现场检测等特点。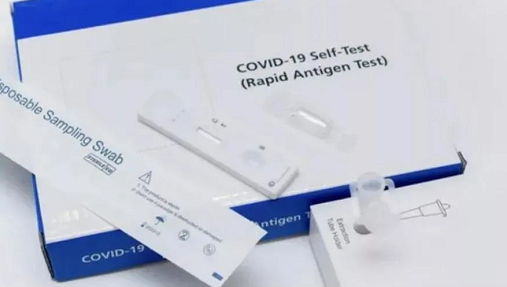
抗原检测盒确实能进行自我筛查,尤其在出现咳嗽、发热等症状时,对是否感染新冠病毒进行筛查较为敏感。但是,抗原检测盒较难发现感染初期或无症状感染者,对感染初期或无症状感染者的漏检率较高。
根据我国的“动态清零”目标,始终坚持发现一起疫情就迅速扑灭一起疫情,需要能第一时间发现感染初期和无症状感染者。因此,使用核酸检测试剂更有针对性,也是我国采用最高效率、最低成本、最短时间来控制疫情的最好办法。国内新冠快速自测试剂盒企业
国内研产新冠快速自测试剂盒的企业也是剑指海外市场。当前国内有11家企业旗下在海外获批上市的新冠自测盒产品,其中3家获得FDA-EUA授权,未上市的艾康生物最早获批,九安医疗是第一家获批的上市公司,东方生物则是作为西门子医疗抗原自测产品的指定授权供应商。另外,万泰生物、万孚生物、美康生物都正在申请美国FDA认证。
1月14日,九安医疗发布公告表示,其美国子公司iHealthLabs.Inc和美国ACC(美国陆军合约管理指挥部)于当地时间2022年1月13日签订了《采购合同》,向其销售 iHealth试剂盒产品,合同价税合计金额为12.75亿美元,约合人民币81亿元,已超过公司2020年度经审计主营业务收入的50%(人民币10.04亿元)。据九安医疗此前披露的一份问询函回复,每个检测盒的采购价格为5美元,这意味着此次美国附加的订单金额约为25亿美元,而如果每月所有美国人都需要做检测,26亿份检测盒的订单将高达130亿美元。截至目前,欧洲有25家以上的抗原检测供应商,而通过认证的美国抗原家庭自测产品供应商仅12家,率先拿到FDA-EUA授权的产品大为受益。九安医疗作为首个获批的“中国制造”上市公司,且已拿到多张采购订单,自然获得资本倾注。国内核酸检测公司对于“出海”如饥似渴,但美国政府则占据支配地位。1月14日晚间,九安医疗发布补充公告表示,公司于当日早盘前披露的《关于美国子公司签订日常经营重大合同的公告》,美国政府有权随时因自身因素中止该合同,具体而言就是美国政府可以不需要理由在合同的执行过程中要求停止执行,且取消后续的采购,卖方需承担相应的风险及可能产生的损失。国内企业间的竞争之外,美国本土的雅培、 罗氏、西门子等都有获批的快速检测试剂盒,虽然部分企业的断货风波留给了国内企业突围的窗口期,但这个时间不会太长,而国内企业的产能也会在突然涌入的大订单面前接受考验。核酸自测试剂盒行业以后是否会陷入“内卷”,让我们拭目以待。文章部分内容来源于网络,由微粉网整理,贵在分享,如有侵权请告知删除!






